12 வது இயற்பியல் :அலகு 9 : அணு மற்றும் அணுக்கரு இயற்பியல்
கதிரியக்க சிதைவு விதி
கதிரியக்க சிதைவு விதி
முந்தைய பகுதியில் ஒரு தனித்த கதிரியக்க அணுக்கருவின்
சிதைவுப் பாங்கினைப் பற்றி அறிந்தோம். நடைமுறையில் கதிரியக்க தனிமங்கள், மிக அதிக அளவிலான
கதிரியக்க அணுக்கருக்களைக் கொண்டுள்ளது. மேலும் அதிலுள்ள அனைத்து அணுக்கருக்களும் ஒரே
சமயத்தில் சிதைவு அடைவதில்லை என்பதை அறிவோம். ஒரு குறிப்பிட்ட
கால நெடுக்கத்தில் இச்சிதைவு நிகழ்கின்றது.
மேலும் இச்சிதைவு ஒரு ஒழுங்கற்ற நிகழ்வாகும் (random process). எந்த நொடியில், எந்த
அணுக்கரு சிதைவடையும் என்பதை நம்மால் முன்கூட்டியே கணிக்க இயலாது. மாறாக (ஒரு நாணயத்தை
சுண்டுவது போல்) நிகழ்தகவு அடிப்படையில்தான் நம்மால் கணக்கிட முடியும். கதிரியக்கத்
தனிமம் ஒன்றில் ஒரு குறிப்பிட்ட கால இடைவெளியில் எத்தனை அணுக்கருக்கள் சிதைவடைந்துள்ளன
என்பதைத் தோராயமாகக் கணக்கிடலாம்.
ஒரு குறிப்பிட்ட கணத்தில், ஓரலகு நேரத்தில்
நடைபெறும் சிதைவுகளின் எண்ணிக்கை (சிதைவு வீதம் [dN/dt]) ஆனது, அக்கணத்தில் உள்ள அணுக்கருக்களின்
எண்ணிக்கைக்கு (N) நேர்த்தகவில் இருக்கும்.
அதாவது, dN / dt ∝ N
தகவு மாறிலியை அறிமுகப்படுத்தினால், இச்சமன்பாட்டினைப்
பின்வருமாறு எழுதலாம்,

இங்கு பயன்படுத்தப்படும் தகவு மாறிலி என்பது
சிதைவு மாறிலி என்றழைக்கப்படும்; வெவ்வேறு கதிரியக்கப் பொருள்களுக்கு λ இன்
மதிப்பு வெவ்வேறாக இருக்கும். மேலும், இச்சமன்பாட்டில் வரும் எதிர்க்குறியானது நேரம்
செல்லச்செல்ல அணுக்கருக்களின் எண்ணிக்கை Nஇன் மதிப்பு குறையும் என்பதைக் காட்டுகிறது.
சமன்பாடு (8.32)ஐ வேறு விதமாக எழுதினால்,

இங்கு dN என்பது dt நேர இடைவெளியில் சிதைவடையும்
அணுக்கருக்களின் எண்ணிக்கையைக் குறிக்கும். t = 0 நேரத்தில் (அதாவது ஆரம்ப நேரத்தில்)
உள்ள அணுக்கருக்களின் எண்ணிக்கை N0 என்க. சமன்பாடு (8.33)ஐத் தொகையீடு செய்யும்போது,
எந்தவொரு கணத்திலும் உள்ள அணுக்கருக்களின் எண்ணிக்கையைக் கணக்கிடலாம். சமன்பாடு
(8.33) இலிருந்து,

இருபுறமும் அடுக்குக்குறி மதிப்பைப் பெற, நமக்குக்
கிடைப்பது

(குறிப்பு:
சமன்பாடு (8.35) கதிரியக்கச் சிதைவு விதி எனப்படும்.
இங்கு N என்பது t நேரத்திற்கு பிறகு, சிதைவடையாமல் இருக்கும் அணுக்கருக்களின் எண்ணிக்கை
மற்றும் N0 என்பது t=0 நேரத்தில் உள்ள அணுக்கருக்களின் எண்ணிக்கை ஆகும்.
நேரம் ஆக ஆக அணுக்களின் எண்ணிக்கை அடுக்குக்குறி முறைப்படி குறையும் என்பதை இச்சமன்பாட்டிலிருந்து
நாம் அறிந்து கொள்ளலாம். அனைத்து கதிரியக்க அணுக்கருக்களும் சிதைவடைய முடிவிலா காலம்
(infinte) ஆகும் என்பதை இதன் மூலமாக நாம் அறியலாம். சமன்பாடு (8.35) ஆனது படம்
8.26ல் வரைபடமாகக் காட்டப்பட்டுள்ளது.

படம் 8.26 கதிரியக்கச் சிதைவு விதி
(கதிரியக்கச்) செயல்பாடு (Activity) அல்லது
சிதைவு வீதம் என்ற மற்றுமொரு பயனுள்ள அளவீட்டை நாம் வரையறுக்கலாம். அதாவது, (கதிரியக்கச்)
செயல்பாடு அல்லது சிதைவு வீதம் (R) என்பது ஒரு வினாடியில் சிதைவடையும் அணுக்கருக்களின்
எண்ணிக்கை ஆகும். இது
dN / dt என குறிக்கப்படுகிறது. R என்பது ஒரு
நேர்க்குறி மதிப்புடைய அளவீடு ஆகும்.
சமன்பாடு (8.35) இலிருந்து,
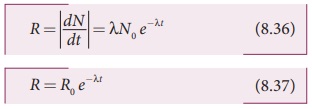
இங்கு R0 = λN0
சமன்பாடு (8.37)-உம் கதிரியக்கச் சிதைவு விதிக்கு
இணையானதே. இங்கு R0 என்பது t = 0 நேரத்தில் கதிரியக்கப் பொருளின் செயல்பாடு
மற்றும் R என்பது t நேரத்தில் அதன் செயல்பாடு ஆகும். சமன்பாடு (8.37)லிருந்து கதிரியக்கச்
செயல்பாடும் அடுக்குக் குறியீட்டு அடிப்படையில் சிதைவடையும் தன்மை கொண்டது என்பது தெரிகிறது.
எந்தவொரு கணம் -இலும் அக்கணத்தில் சிதைவடையாமல் இருக்கும் அணுக்களின் எண்ணிக்கையை வைத்து
கதிரியக்கச் செயல்பாட்டை (R) எழுதலாம்.
N = N0e−λt ஆகையால், சமன்பாடு (8.37) லிருந்து,

சமன்பாடு (8.38)-இன்படி, எந்தவொரு கணம் t-யிலும்
கதிரியக்கச் செயல்பாடானது அக்கணத்தில் உள்ள சிதைவடையா அணுக்கருக்களின் எண்ணிக்கை N
மற்றும் சிதைவு மாறிலி λ ஆகியவற்றின் பெருக்கற்பலனுக்கு
சமமாகும். நேரத்தைப் பொருத்து N குறைந்து கொண்டே இருப்பதால், R-ம் குறைந்து கொண்டே
இருக்கும்.
கதிரியக்கச்செயல்பாட்டின் SI அலகு பெக்கரல்
(Bq). மேலும் ஒரு பெக்கரல் என்பது ஒரு வினாடிக்கு ஒரு சிதைவைத் தரும் தனிமத்தின் செயல்பாட்டைக்
குறிக்கும். கதிரியக்கச் செயல்பாட்டிற்கு மற்றொரு கியூரி (Ci) என்ற அலகும் உள்ளது.
1 கியூரி =1 Ci =3.7x1010 சிதைவுகள்
/ வினாடி
1 Ci = 3.7x1010 Bq
குறிப்பு
ஒரு கியூரி என்பது 1 g ரேடியம் 1 வினாடியில் உமிழும் சிதைவுகளின்
எண்ணிக்கைக்குச் சமமாகும்; அதாவது ஒரு வினாடிக்கு 3.7x1010 சிதைவுகள்.