11 வது வேதியியல் : அலகு 2 : அணுவின் குவாண்டம் இயக்கவியல் மாதிரி
கணக்குகளுக்கான தீர்வுகள்
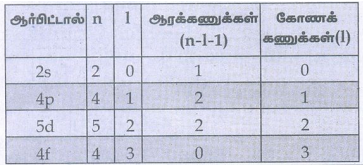
28. 2s, 4p, 5d மற்றும் 4f ஆர்பிட்டால்களுக்கு எத்தனை ஆரக் கணுக்கள் (radial node) காணப்படுகின்றன? எத்தனை கோணக் கணுக்கள் (angular nodes) காணப்படுகின்றன.
29. சரிபாதியளவு நிரப்பப்பட்ட ஆர்பிட்டால்கள் நிலைப்புத்தன்மை பெறுதல் p - ஆர்பிட்டாலைக் காட்டிலும் d - ஆர்பிட்டாலில் அதிகமாக உள்ளது. ஏன்?
"பரிமாற்ற ஆற்றல் அதிகரிக்கும் போது ஆர்பிட்டால்களின் நிலைப்புத்தன்மை அதிகரிக்கிறது”
d − ஆர்பிட்டால்களின் ஒட்டு மொத்த எலக்ட்ரான் பரிமாற்றங்கள் = 10
p − ஆர்பிட்டால்களின் ஒட்டு மொத்த எலக்ட்ரான் பரிமாற்றங்கள் = 3
எனவே சரிபாதியளவு நிரப்பப்பட்ட d−ஆர்பிட்டால்கள் அதிக நிலைப்புத்தன்மை பெறுகின்றன.
30. பின்வரும் d5 எலக்ட்ரான் அமைப்புகளைக் கருதுக.
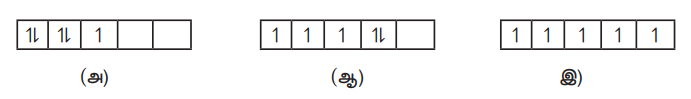
(i) இவற்றுள் சிறும ஆற்றல் நிலையை குறிப்பிடுவது எது?
(i) அதிகபட்ச பரிமாற்ற ஆற்றலைப் பெற்றுள்ள அமைப்பு எது?
(i) கொடுக்கப்பட்ட மூன்று d5 எலக்ட்ரான் அமைப்புகளுள், அமைப்பு (இ) சிறும ஆற்றல் நிலையைக் குறிப்பிடுகிறது.
(ii) அதிகபட்ச பரிமாற்ற ஆற்றலைப் பெற்றுள்ள அமைப்பும், அமைப்பு (இ) ஆகும்.
31. பௌலி தவிர்க்கைத் தத்துவத்தினைக் கூறு
ஒரு அணுவிலுள்ள எந்த இரு எலக்ட்ரான்களுக்கும், அவற்றின் நான்கு குவாண்டம் எண்களின் மதிப்பின் தொகுப்பும் ஒன்றாக இருக்காது.
32. ஆர்பிட்டால் வரையறு. 3px மற்றும் 4dx2– y2 ஆர்பிட்டாலில் உள்ள எலக்ட்ரானுக்கு n மற்றும் l மதிப்புகளைக் கூறுக.
எலக்ட்ரான்களை காண்பதற்கு அதிகபட்ச நிகழ் தகவினைப் பெற்றுள்ள முப்பரிமாண வெளி ஆர்பிட்டால் எனப்படும்.

33. காலத்தைச் சார்ந்து அமையாத ஷ்ரோடிங்கர் அலைச்சமன்பாட்டினை சுருக்கமாக விளக்குக.
ஹெய்சன்பர்க் நிச்சயமற்ற கொள்கை மற்றும் நுண் துகளின் ஈரியல்புத் தன்மையை அடிப்படையாகக் கொண்டு, ஷ்ரோடிங்கர் எலக்ட்ரானின் அலைப் பண்பினை ஒரு வகைக்கெழுச் சமன்பாட்டின் அடிப்படையில் குறிப்பிட்டார்.
இது எலக்ட்ரான் இயங்கக்கூடிய விசையின் புலத்தைப் பொறுத்து, புறவெளியில் அலைச்சார்பில் ஏற்படும் மாறுபாட்டைத் தீர்மானிக்கிறது, அதாவது,

இச்சமன்பாட்டில், காலம் (t) ஒரு சார்பாக இடம் பெறவில்லை. எனவே, இச்சமன்பாடு காலத்தைப் பொறுத்து அமையாத ஷ்ரோடிங்கரின் அலைச் சமன்பாடு எனப்படுகிறது.
34. Δv = 0.1% மற்றும் V = 2.2 × 106 ms-1 ஆக உள்ள எலக்ட்ரான் ஒன்றின் நிலையை அளவிடுவதில் உள்ள நிச்சயமற்றத் தன்மையினைக் கணக்கிடுக.

∆x ≥ 2.635 × 10−8 m
35. O - அணுவில் உள்ள 8வது எலக்ட்ரான் மற்றும் Cl - அணுவில் உள்ள 15வது எலக்ட்ரான் ஆகியவற்றிற்கான நான்கு குவாண்டம் எண்களின் மதிப்புகளையும் தீர்மானிக்கவும்.

36. குவாண்டம் இயக்கவியலின் அடிப்படையில் ஹைட்ரஜன் அணுவின் ஆற்றல் மதிப்பு
En = (-13.6 / n2) eV atom-1
i) இதனைப் பயன்படுத்தி n = 3 மற்றும் n = 4க்கு இடையேயான ஆற்றல் வேறுபாடு ΔE யைக் கண்டறிக.
ii) மேற்கண்டுள்ள பரிமாற்றத்திற்கு உரிய அலை நீளத்தினைக் கணக்கிடுக.
(i) E3 = −13.6/ 32 = − 1.51 eV அணு−1
E4 = −13.6/ 42 = − 0.85 eV அணு−1
∆E = (E4 − E3) = (−0.85) − (−1.51) = 0.66 eV அணு−1
[∵1eV = 1.6 × 10−19J]
(ii) ஆற்றல் வேறுபாடு ∆E = 0.66 eV அணு−1
= 0.66 × 1.6 × 10−19J
= 1.06 × 10−19J
= hγ
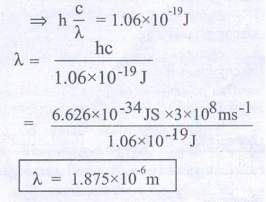
λ = 1.875 × 10−6m
37. 5400 Å பச்சை நிற ஒளியின் அலை நீளத்திற்கு சமமான டிபிராக்ளி அலைநீளத்தினைப் பெற 54g டென்னிஸ் பந்து எவ்வளவு வேகத்தில் பயணிக்க வேண்டும்?
λ = 5400Å = 5400 × 10−10 m;
m = 54g = 54 × 10−3 Kg ; V = ?
λ = h/mV ; V = h/mλ =
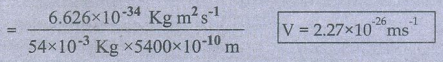
V = 2.27 × 10−26 ms−1
38. பின்வரும் ஒவ்வொன்றிற்கும், துணைக்கூட்டின் குறியீடு, அனுமதிக்கப்பட்ட m மதிப்புகள் மற்றும் ஆர்பிட்டால்களின் எண்ணிக்கையினைத் தருக.
i) n = 4, l =2,
ii) n = 5, l = 3
iii) n = 7, l = 0

39. Mn2+ மற்றும் Cr3+ ஆகியனவற்றின் எலக்ட்ரான் அமைப்புகளைத் தருக.
Mn2+ மற்றும் Cr3+ ன் e− அமைப்புகள்
25Mn2+ (23 e- கள்) : 1s2 2s2 2p6 3s2 3p6 4s0 3d5
24Cr3+ ( 21 e− கள்) : 1s2 2s2 2p6 3s2 3p6 4s0 3d3
40. ஆஃபா தத்துவத்தினை விவரிக்க.
அடி ஆற்றல் நிலையிலுள்ள அணுவின் ஆர்பிட்டால்கள் அவற்றின் ஆற்றல்களின் ஏறுவரிசையில் நிரப்பப்படுகின்றன. அதாவது எலக்ட்ரான்கள் குறைவான ஆற்றலுடைய ஆர்பிட்டால் முழுமையாக நிரப்பப்பட்ட பின்னரே அடுத்த உயர் ஆற்றலுடைய ஆர்பிட்டாலினுள் நுழையும்.
41. ஒரு அணுவானது 35 எலக்ட்ரான்கள் மற்றும் 45 நியூட்ரான்களைக் கொண்டுள்ளது.
i) புரோட்டான்களின் எண்ணிக்கை
ii) தனிமத்தின் எலக்ட்ரான் அமைப்பு
iii) கடைசி எலக்ட்ரானின் நான்கு குவாண்டம் எண்களின் மதிப்பு ஆகியனவற்றை கண்டறிக.
35 எலக்ட்ரான்கள், 45 நியூட்ரான்களைக் கொண்ட அணுவின்
(i) புரோட்டான்களின் எண்ணிக்கை = 35
(ii) எலக்ட்ரான் அமைப்பு = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
(iii) கடைசி எலக்ட்ரானின் 4p5 ன் 4 குவாண்டம் எண் மதிப்புகள் 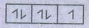
n = 4; 1 = 1; m = 0; s = − ½
42. ஹைட்ரஜன் அணுவின் போர் வட்டப்பாதையின் சுற்றளவானது, அணுக்கருவினைச் சுற்றி வரும் எலக்ட்ரானுக்கான டிபிராக்ளி அலைநீளத்தின் முழு எண் மடங்கிற்குச் சமம் எனக் காட்டுக.
நிரூபிக்க வேண்டியது:
எலக்ட்ரான் சுற்றி வரும் வட்டப்பாதையின் சுற்றளவானது, அதன் அலைநீளத்தின் முழு எண் மடங்காக இருக்க வேண்டும்.
அதாவது, வட்டப்பாதையின் சுற்றளவு 2πr = nλ.
n = 5 எனில்
2πr = 5λ

43. பின்வரும் செயல்முறைக்குத் தேவைப்படும் ஆற்றலைக் கணக்கிடுக.
He+ (g) → 2He2+ (g) + e-
சிறும ஆற்றல் நிலையில் உள்ள ஹைட்ரஜனின் அயனியாக்கும் ஆற்றல் -13.6 ev atom-1.
He+(g) → He2+(g)+ e−
E = ?
(H ன் அயனியாக்கும் ஆற்றல் = 13.6 evatom−1)
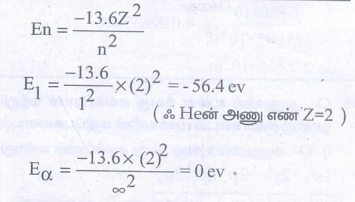
கொடுக்கப்பட்ட செயல்முறைக்கு தேவைப்படும். ஆற்றல் = E∞ − E1 = 0 − (−56.4) = 56.4 eV
44. நிறை எண் 37 உடைய ஒரு அயனி ஒற்றை எதிர்மின் சுமையினைப் பெற்றுள்ளது. இந்த அயனியானது, எலக்ட்ரான்களைக் காட்டிலும் 11.1% அதிகமான நியூட்ரான்களைப் பெற்றிருந்தால், அந்த அயனியின் குறியீட்டினைக் கண்டறிக.
நிறை எண் 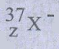 கொண்ட ஒற்றை எதிர்மின் சுமை அயனி என்க.
கொண்ட ஒற்றை எதிர்மின் சுமை அயனி என்க.
எலக்ட்ரான்களின் எண்ணிக்கை = x என்க
ஃபுரோட்டான்களின் எண்ணிக்கை = x − 1
நியூட்ரான்களின் எண்ணிக்கை = எலக்ட்ரான்களை விட 11% அதிகம்
= x + 11.1% x
= x + (11.1/100) x
= 1.11x
⇒ (x − 1) + 1.11x = 37
2.11 x – 1 = 37 ⇒ 2.11x = 38 ⇒ x = 38/2.11 = 18
ஃ அணு எண் Z = புரோட்டானின் எண்ணிக்கை. = x − 1 = 17
எனவே, கொடுக்கப்பட்ட அயனி  ஆகும்.
ஆகும்.
45. Li2+அயனியானது ஹைட்ரஜனை ஒத்த அயனியாகும். அதனை போர் மாதிரியின் அடிப்படையில் விவரிக்க இயலும். அதன் மூன்றாம் வட்டப்பாதையின் போர் ஆரம் மற்றும் நான்காம் வட்டப்பாதையில் உள்ள ஒரு எலக்ட்ரானின் ஆற்றல் ஆகியவற்றைக் கண்டறிக.
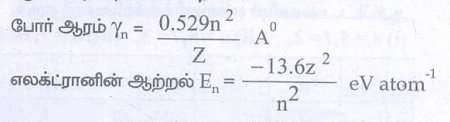
Li2+ அயனியின் அணு எண் = 3 ; e− களின் எண்ணிக்கை = 1
i) 3வது வட்டப்பாதையில் போர் ஆரம் r3 = 0.529(3)2 /3 = 1.587 Å
ii) 4வது வட்டப்பாதையில் எலக்ட்ரானின் ஆற்றல்
E4 = −13.6(3)2/ 42 = −7.65 eV atom−1
46. துகள் முடுக்கிகளைக் கொண்டு புரோட்டான்களை முடுக்குவிக்க இயலும். அத்தகைய முடுக்குவிக்கப்பட்ட 2.85 × 108 ms-1 வேகத்தில் இயங்கும் புரோட்டான் ஒன்றின் அலை நீளத்தினை (Åல்) கணக்கிடுக. (புரோட்டானின் நிறை 1.673 × 10-27Kg).
V = 2.85 × 108 ms−1
mp = 1.673 × 10−27 kg
λ = ?
λ = h/mv

λ = 1.389 × 10−15m (or) 1.389 × 10−5 Å
47. 140 km hr-1 வேகத்தில் பயணிக்கும் 160 g நிறையுடைய கிரிக்கெட் பந்து ஒன்றின் டிபிராலி அலைநீளம் (cmல்) கணக்கிடுக.
V = 140 kmhr−1 = (140 × 1000)/3600 ms−1 = 38.88ms−1
m = 160g = 160 × 10−3 Kg ;
தீர்வு:
λ = h/mv
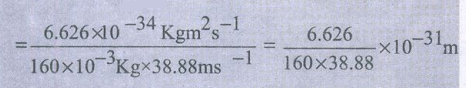
= 1.065 × 10−34 m
λ = 1.065×10−32 cm
48. ஆர்பிட்டில் உள்ள ஒரு எலக்ட்ரானின் நிலையினைத் தீர்மானிப்பதில் உள்ள நிச்சயமற்றத் தன்மை 0.6 Å என இருக்குமெனில், அதன் உந்தத்தில் ஏற்படும் நிச்சயமற்றத் தன்மை யாது?
∆x = 0.6 Å; ∆p = ?
∆x . ∆p ≥ h/4π
0.6 × 10−10 m × ∆p ≥ (6.626 × 10−34)/4π
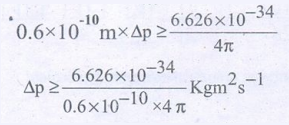
∆p ≥ 0.879 × 10−24 Kgms−1
49. துகள் ஒன்றின் நிலையில் ஏற்படும் நிச்சயமற்றத் தன்மையின் அளவீடானது அதன் டீபிராக்ளி அலைநீளத்திற்குச் சமம் எனில், அதன் திசைவேகத்தில் ஏற்படும் குறைந்த பட்ச நிச்சயமற்றத் தன்மை அதன் திசைவேகத்தின் 1 / 4π மடங்குக்குச் சமம் எனக் காட்டுக.
ஹெய்சன்பர்க் − ன் நிச்சயமற்றத் தன்மைக்கான சமன்பாடு ∆x ∆p ≥ h/4π
கொடுக்கப்பட்டுள்ளபடி ∆x = λ எனில், λ m ∆V ≥ h/4π

⇒ ∆V ≥ V/4π நிரூபிக்கப்பட்டது.
50. அமைதி நிலையில் உள்ள ஒரு எலக்ட்ரான் 100V மின்னழுத்த வேறுபாட்டைக் கொண்டு முடுக்குவிக்கப்படும் போது, அந்த எலக்ட்ரானின் டிபிராக்ளி அலைநீளத்தைக் கண்டறிக.
மின்னழுத்த வேறுபாடு = 100V = 100 × 1.6 × 10−19 J = 1.6 × 10−17 J
λ = h/ √2meV
λ = ?
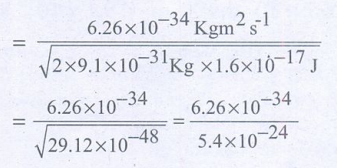
λ = 1.227 × 10−10 m (or) 1.227 Å
51. விடுபட்ட குவாண்டம் எண்கள் / துணை ஆற்றல் மட்டங்களைக் கண்டறிக.

விடை
