வளம், இயற் பண்புகள், போரானின் வேதிப் பண்புகள், போரானின் பயன்கள் - தொகுதி 13 (போரான் தொகுதி) தனிமங்கள் | 12th Chemistry : UNIT 2 : p-Block Elements-I
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 2 : p-தொகுதி தனிமங்கள்-I
தொகுதி 13 (போரான் தொகுதி) தனிமங்கள்
தொகுதி 13 (போரான் தொகுதி) தனிமங்கள்:
வளம்:
போரான் , பொதுவாக போரேட்டுகளாக காணப்படுகிறது. அதன் முக்கிய தாதுக்கள் போராக்ஸ் – Na2[B4O5 (OH)4].8H2O மற்றும் கெர்னைட் – Na2[B4O5 (OH)4].2H2O.ஆகியனவாகும். அலுமினியம் மிக அதிகளவில் காணப்படும் உலோகமாகும், இது ஆக்சைடுகளாகவும், அலுமினோசிலிக்கேட் பாறைகளிலும் காணப்படுகிறது.அலுமினியத்தின் முதன்மையானதாதுவான பாக்சைட் (A12O3.2H2O) லிருந்து அலுமினியம் வணிக ரீதியாக பிரித்தெடுக்கப்படுகிறது. இந்த தொகுதியின் மற்ற தனிமங்கள் மிகக்குறைந்த அளவிலேயே கிடைக்கின்றன. Ga, In மற்றும் TI போன்ற மற்ற தனிமங்கள் அவற்றின் சல்பைடுகளாக கிடைக்கின்றன.
இயற் பண்புகள்:
13 ஆம் தொகுதித் தனிமங்களின் சில இயற் பண்புகள் கீழே அட்டவணைப்படுத்தப்பட்டுள்ளன.
அட்டவனை 2.3 13 ஆம் தொகுதித் தனிமங்களின் சில இயற் பண்புகள்
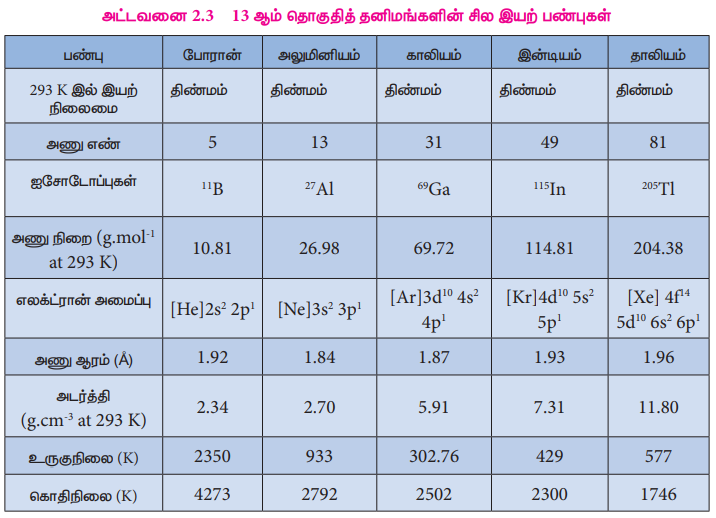
போரானின் வேதிப் பண்புகள்:
இந்தத் தொகுதியிலுள்ள ஒரே அலோகம் போரான் மட்டுமே, மேலும் இது வினைதிறன் குறைந்தது. எனினும், உயர் வெப்பநிலைகளில் போரான் அதிக வினைத்திறனைக் காட்டுகிறது. போரானின் பெரும்பாலான சேர்மங்கள் எலக்ட்ரான் குறைச் சேர்மங்களாகும், போரானின் சிறிய உருவளவு, உயர் அயனியாக்கும் ஆற்றல் மற்றும் கார்பன், ஹைட்ரஜன் ஆகியவற்றை ஒத்த எலக்ட்ரான் கவர்திறன் மதிப்பு ஆகிய காரணங்களால் வழக்கத்திற்கு மாறான புதிய வகை சகப்பிணைப்புகளை உருவாக்குகின்றன.
உலோக போரைடுகள் உருவாதல்:
கார உலோகங்களைத் தவிர மற்ற பெரும்பாலான உலோகங்கள் MxBy (x மதிப்பு 11 வரையிலும், y மதிப்பு 66 அல்லது அதற்கும் அதிகமாக இருக்கும்) எனும் பொதுவாய்ப்பாட்டைக் கொண்ட போரைடுகளை உருவாக்குகின்றன.
போரான் உடன் உலோகங்களின் நேரடி இணைதல்:

போரான் ட்ரைஹேலைடுகளின் ஒடுக்கம்:
ஹைட்ரஜன் உதவியுடன், உலோகத்தை கொண்டு போரான்ட்ரைகுளோரைடை ஒடுக்கும்போது உலோக போரைடுகள் கிடைக்கின்றன.
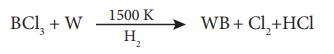
ஹைட்ரைடுகள் உருவாதல்:
போரான் நேரடியாக ஹைட்ரஜனுடன் வினை புரிவதில்லை , எனினும் போரேன்கள் (boranes) எனும் புதுவகை ஹைட்ரைடுகளை உருவாக்குகிறது. டைபோரேன்- B2H6 ஒரு எளிய போரேன் ஆகும். டைபோரேனிலிருந்து மற்ற உயர் போரேன்களை உருவாக்க இயலும். வாயுநிலையிலுள்ள போரான்ட்ரைபுளூரைடை, 450K வெப்பநிலையில், சோடியம் ஹைட்ரைடுடன்வினைப்படுத்தும்போது டைபோரேன் கிடைக்கிறது. அதைத் தொடர்ந்து நிகழும் வெப்பச்சிதைவை தடுக்கும்பொருட்டு டைபோரேன் விளைபொருளானது உடனடியாக நீக்கப்படுகிறது.
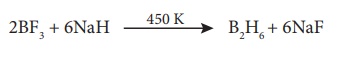
போரான் ட்ரைஹேலைடுகள் உருவாதல்:
போரான், உயர் வெப்பநிலைகளில் ஹேலஜன்களுடன் இணைந்து போரான் ட்ரைஹேலைடுகளை உருவாக்குகிறது.
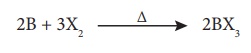
போரான் நைட்ரைடு உருவாதல்:
போரான், உயர் வெப்பநிலைகளில் டைநைட்ரஜனுடன் எரிந்து போரான் நைட்ரைடை உருவாக்குகிறது.

ஆக்சைடுகள் உருவாதல்:
ஏறத்தாழ 900K வெப்பநிலையில் ஆக்ஸிஜனுடன் வினைப்படுத்தும்போது போரான், அதன் ஆக்ஸைடை உருவாக்குகிறது.
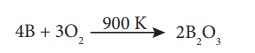
அமிலங்கள் மற்றும் காரங்களுடன் வினை:
ஹேலோ அமிலங்களுடன் போரான் வினைபுரிவதில்லை . எனினும், சல்ஃபியூரிக் அமிலம் மற்றும் நைட்ரிக் அமிலம் போன்ற ஆக்ஸிஜனேற்ற காரணிகளுடன் வினைப்பட்டு போரிக் அமிலத்தை உருவாக்குகிறது.
2B + 3H2 SO4 → 2H3 BO3 + 3SO2
B + 3HNO3 → H3 BO3 + 3NO2
போரான் , உருகிய சோடியம் ஹைட்ராக்சைடுடன் வினைப்பட்டு சோடியம் போரேட்டைத் தருகிறது.
2B + 6NaOH → 2Na3BO3 + 3H2
போரானின் பயன்கள்:
1. போரான், நியுட்ரான்களைக் உறிஞ்சும் திறனைப் பெற்றுள்ளதால் அதன் 10B5 ஐசோடோப்பானது அணு உலைகளில் மட்டுப்படுத்தியாக பயன்படுகிறது.
2. படிகவடிவமற்ற போரான் - ராக்கெட் எரிபொருள் எரியூட்டியாக பயன்படுகிறது.
3. போரான், தாவர செல் சுவரின் முக்கிய பகுதிப் பொருளாக உள்ளது.
4. போரான் சேர்மங்கள் பல்வேறு பயன்பாடுகளை பெற்றுள்ளன. எடுத்துக்காட்டாக, கண் மருந்துகள், புரைதடுப்பான்கள், சலவைத் தூள் ஆகியவற்றில் போரிக் அமிலம் மற்றும் போராக்ஸ் உள்ளன. பைரக்ஸ் கண்ணாடி தயாரிப்பில் போரிக் அமிலம் பயன்படுகிறது.